คุณสมบัติโอโซน

คุณสมบัติ
ก๊าซโอโซนบริสุทธิ์จะมีสีน้ำเงินแก่ มีกลิ่นคล้ายคลอรีนจางๆ ถ้าดมเข้าไปมากๆ จะปวดศีรษะ โอโซนละลายน้ำได้มากกว่าก๊าซออกซิเจน มีจุดเดือดที่ -111.5 องศาเซลเซียส และมีจุดหลอมเหลวที่ -251 องศาเซลเซียส
เมื่ออยู่ในสภาวะที่เป็นก๊าซบริสุทธิ์จะเสถียรภาพดีพอสมควร
แต่ถ้ามีสารอินทรีย์ปนอยู่ในน้ำแล้ว โอโซนจะสลายตัวเป็นออกซิเจนได้ง่าย ถ้าผสมอยู่กับอากาศจะค่อยๆกลายเป็นออกซิเจน ถ้าอุณหภูมิถึง 300 องศาเซลเซียส จะสลายตัวอย่างรวดเร็ว
แหล่งที่มา
1. เกิดตามธรรมชาติ
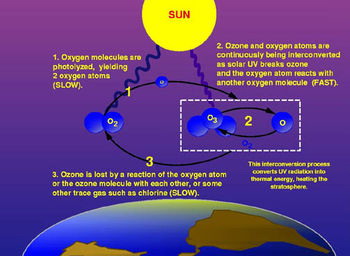
เกิดจากการรวมตัวกันของโมเลกุลของก๊าซออกซิเจน โดยมีรังสีอุลตราไวโอเลตที่มีความยาวคลื่นน้อยกว่า 242 นาโนเมตร เป็นตัวเร่งปฏิกิริยา ทำให้เกิดพลังงานที่จะดึงเอาโมเลกุลของก๊าซออกซิเจนให้แตกตัวเป็นอะตอมของออกซิเจน 2 อะตอม และเมื่ออะตอมของออกซิเจน 1 อะตอมพบกับโมเลกุลของก๊าซออกซิเจนจะเกิดการรวมตัวดังสมการ
O2 ---- (uv) ----- O+O
O+O2 ---- O3
โอโซนที่เกิดขึ้นนี้สามารถดูดกลืนรังสีอัลตราไวโอเลตแล้วแตกตัวกลายเป็นก๊าซออกซิเจนและรวมตัวกับอะตอมของออกซิจน กลายเป็นโอโซนได้อีก โดยมีรังสีอัลตราไวโอเลตเป็นตัวเร่งปฏิกิริยาซึ่งจะเกิดเช่นนี้ไปได้เรื่อยๆ โดยไม่มีที่สิ้นสุดแบบปฏิกิริยาลูกโซ่
โอโซนยังสามารถเกิดได้เองในอากาศจากพายุฝนฟ้าคะนองหรือจากฟ้าแลบได้อีกด้วย กระบวนการเกิดปฏิกิริยาดังกล่าวนี้เรียกว่าขบวนการโพโตเคมีคอล(Photochamical process) ซึ่งเป็นปฏิกิริยาที่ทำให้เกิดก๊าซโอโซนและสลายตัวพร้อมกัน และในที่สุดปฏิกิริยาของก๊าซโอโซนก็จะอยู่ในภาวะสมดุลโดยที่อัตราการเกิดและสลายตัวเท่ากัน(แล้วจะเกิดมาทำไมวุ้ย..^_^)
2. เกิดจากการกระทำของมนุษย์
โอโซนถูกผลิตขึ้นมาเพื่อใช้ประโยชน์ในด้านต่าง ๆ เช่น การกำจัดน้ำเสียและใช้ฆ่าเชื้อ การเตรียมก๊าซโอโซนที่สะดวกที่สุดใช้ไฟฟ้า silent electrical discharge กระทำกับอากาศหรือกับก๊าซออกซิเจน ซึ่งกา๊ซออกซิเจนบางส่วนเท่านั้นที่กลายเป็นโอโซน ถ้าใช้อากาศ เรียกก๊าซผสมนี้ว่า ไอโอไนซ์แอร์ (ozonised air) ถ้าใช้ก๊าซออกซิเจนก๊าซโอโซนที่เกิดขึ้นจะปนอยู่กับก๊าซออกซิเจนที่เหลือ เรียกว่า ozonised oxygen เครื่องมือที่ใช้เตรียมก๊าซโอโซนด้วยวิธีนี้เรียกว่า โอโนไนเซอร์ (ozonizer)
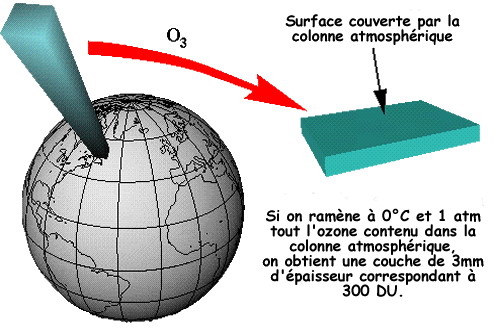
โอโซนเป็นส่วนประกอบของบรรยากาศส่วนหนึ่งที่ปกคลุมผิวโลก ซึ่งมีลักษณะเป็นชั้นบางๆ บริเวณที่อยู่แปรผันอยู่ระหว่างระดับน้ำทะเลขึ้นไปถึงระยะ 60 กิโลเมตร โอโซนส่วนใหญ่อยู่ที่ชั้นบรรยากาศสตาร์โตสเฟียร์ซึ่งพบประมาณร้อยละ 89 - 90 ส่วนที่เหลือจะกระจายอยู่ชั้นโทรโพสเฟียร์และเมโซสเฟียร์
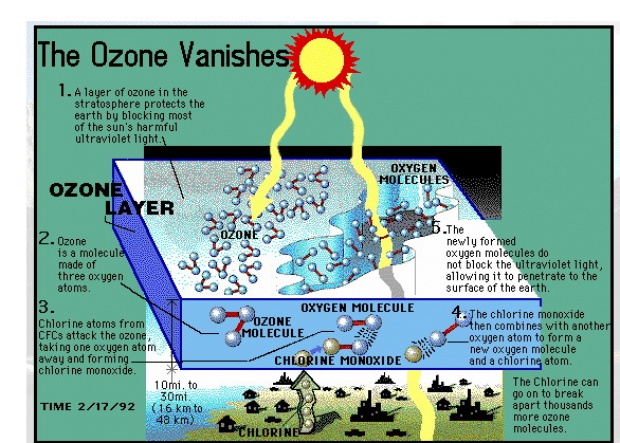
ชั้นโอโซนจะทำหน้าที่กรองแสงอัลตราไวโอเลตจากดวงอาทิตย์โดยสามารถดูดแสง UV-B ความยาวคลื่นระหว่าง 280 - 320 นาโนเมตร ไว้ได้ประมาณ ร้อยละ 70 - 90 รังสี UV-B นี้เป็นอันตรายต่อสิ่งมีชีวิต โอโซนยังมีบทบาทสำคัญในการกำหนดหรือควบคุมอุณหภูมิของโลกและบรรยากาศ
โดยสามารถดูดรังสีอินฟราเรดซึ่งสะท้อนจากผิวโลกและจากชั้นสตราโตสเฟียร์ได้ ทำให้อุณหภูมิบรรยากาศโลกชั้นนี้สูงขึ้น มีผลต่อสภาพภูมิอากาศของผิวโลก
ปริมาณที่ถูกทำลาย
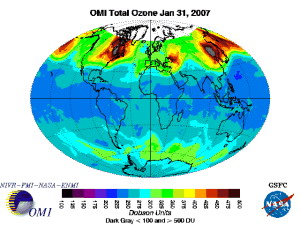
โอโซนส่วนใหญ่อยู่ในบรรยากาศชั้นสตราโตสเฟียร์ โดยมีความเข้มข้นประมาณ 10 ส่วนในล้านส่วน ซึ่งเป็นปริมาณน้อยมากแต่ก็มีความสำคัญต่อสิ่งมีชีวิตต่างๆ ปัจจุบันพบว่ามีการปล่อยสารเคมีต่างๆขึ้นสู่บรรยากาศมากขึ้น ทำให้ก๊าซโอโซนน้อยลงจากการใช้เครื่องมือต่างๆวัดพบว่าโอโซนลดลงร้อยละ 2-3 ที่ระดับความสูง 30-40 กิโลเมตรและจากการใช้เครื่อง สเปคโทรมิเตอร์ (Spectrometer) ตรวจวัดปริมาณโอโซนในบริเวณขั้วโลกได้ของเดือนตุลาคมในทุกปี
ซึ่งเริ่มตั้งแต่ปี 1957 เป็นต้นไป
ก็ได้พบว่าปริมาณของโอโซนที่อยู่เหนือบริเวณขั้วโลกได้ลดลงเกือบ 40 เปอร์เซนต์ และลดลงมากที่สุดในปี 1970 ผลการตรวจวัดระดับโอโซนในบรรยากาศได้รับการยืนยันในปี 1975 จากการใช้ดาวเทียมสำรวจ ได้แสดงให้เห็นว่าเกิดความเสียหายขึ้นต่อชั้นโอโซนเหนือบริเวณขั้วโลกได้ และได้พบความเสียหายได้ขยายตัวมายังบริเวณเส้นศูนย์สูตรประมาณ 45 องศาใต้
ซึ่งองค์การนาซ่าของสหรัฐก็ได้ทำการตรวจสอบสภาพบรรยากาศของโลกได้รายงานว่า เกิดมีลักษณะความเข้มของแสงอาทิตย์ที่ผ่านบรรยากาศไม่สม่ำเสมอจึงได้หาสาเหตุและพบว่าโอโซนที่อยู่รอบโลกในชั้นบรรยากาศโดยเฉพาะบริเวณขั้วโลกใต้ และขั้วโลกเหนือได้ลดลงเป็นหย่อม ๆ และเกิดมากขึ้นเป็นลำดับบางหย่อมคิดเป็นพื้นที่ได้ประมาณ 9 ล้านตารางกิโลเมตร
การที่โอโซนในชั้นสตราโตเพียร์ถูกทำลายไปเนื่องจากสารเคมีที่ปล่อยสู่ชั้นบรรยากาศและสารที่สำคัญคือ CFCs ซึ่งจะมีผลทำให้ UV ส่องมาถึงโลกมากขึ้นมีผลเป็นอันตรายต่อสิ่งมีชีวิตได้
สารเคมี 2 ชนิดที่อยู่ในรูปของก๊าซ
ในชั้นบรรยากาศที่ทำลายโอโซนได้คือคลอรีนออกไซด์(Chlorine Oxides; ClOx) และ ไนโตรเจนออกไซด์ (Nitrogen Oxides ; Nox) (ดูเรื่องสาร CFC ประกอบ)
ไนโตรเจนออกไซด์มาจากไนตรัสออกไซด์ (Nitrous Oxides ; N2O)
ซึ่งมีจุดกำเนิดตามธรรมชาติที่ผิวโลก เช่น กระบวนการ denitrication ของจุลินทรีย์และในบรรยากาศชั้นโทรโพสเฟียร์ เกิดจากฟ้าแลบฟ้าร้อง พวกเครื่องบินที่บินเร็วเหนือเสียง(SST) ที่ปล่อยไนตริกออกไซด์จากไอเสียและยังมีสารพวกฮาโลเจน (Halogen) โดยเฉพาะพวกก๊าซโบมีน(Br) ที่สามารถสลายโอโซนได้ในทางทฤษฎี
ขบวนการสำคัญที่สุด
ที่ทำลายโอโซนคือขบวนการที่มีอะตอมของคลอรีน ไนตริกออกไซด์ ไฮโดรเจนออกไซด์ โบมีน และ ไฮรโดรเจนเป็นตัวเร่งปฏิกิริยา (catalyst) ผลของปฏิกิริยาที่ทำกับโอโซนหรือออกซิเจนนั้น จะทำให้อะตอมของสารพวกนั้นออกมาและเริ่มต้นใหม่เป็นวงจร ดังนี้
O3 + Solar radiation---------------- O + O2
O + XO3 --------------------- X + O2
X + O3 --------------------- XO + O2
------------------------------------------------------------------------------------------------
Net 2O3 3O2
(X = Cl,No,Br,OH,H)
ขอขอบคุณ ข้อมูลที่มีประโยชน์จาก เว็บไซต์ กิตติยาดอทคอม
เพื่อร่วมกันสร้างสังคมแห่งการเรียนรู้บนโลกอินเตอร์เน็ต
ผู้มีบทความทางด้านวิทยาศาสตร์น่ารู้
สามารถส่งผลงานของท่านมาได้ที่ arunee@teeneemedia.com


 กระทู้ร้อนแรงที่สุดของวันนี้
กระทู้ร้อนแรงที่สุดของวันนี้
























 กระทู้ล่าสุด
กระทู้ล่าสุด


 รูปเด่นน่าดูที่สุดของวันนี้
รูปเด่นน่าดูที่สุดของวันนี้
















































Love illusion ความรักลวงตา เพลงที่เข้ากับสังคมonline
Love illusion Version 2คนฟังเยอะ จนต้องมี Version2กันทีเดียว
Smiling to your birthday เพลงเพราะๆ ไว้ส่งอวยพรวันเกิด หรือร้องแทน happybirthday